Асептический некроз таранной кости голеностопного сустава на мрт
Содержание:
- Стадии асептического некроза таранной кости. Лечение некроза таранной кости голеностопного сустава в Москве
- Методы лечения
- Диагностика и лечение патологии
- Причины
- Важные факты о синдроме запястного канала
- Локализация асептического остеонекроза.
- Диагностика асептического некроза полулунной кости
- Классификация
- Лечение
- Диагностика асептического некроза полулунной кости
- Симптоматика
- Кинбека болезнь
- Диагноз
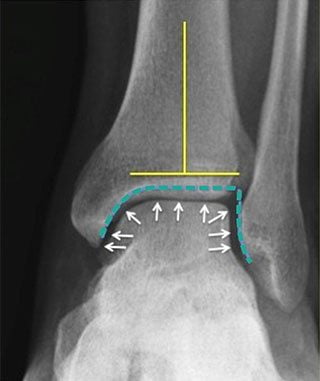
Стадии асептического некроза таранной кости. Лечение некроза таранной кости голеностопного сустава в Москве
Суставы при ходьбе и беге принимают вес тела, и ежедневно подвергаются большой нагрузке. При неудачной постановке стопы или падении на прямые ноги случается внутрисуставной перелом. Повреждение сосудов в суставном хряще или окклюзии артерий, характерная для ряда заболеваний, приводит к иннервации кровоснабжения и развитию некроза таранной кости. В начале процесса ткани отмирают локально, затем патологический процесс распространяется на всю кость. При отсутствии своевременного лечения некроза голеностопного сустава пациенту грозят обездвиживание и инвалидность.
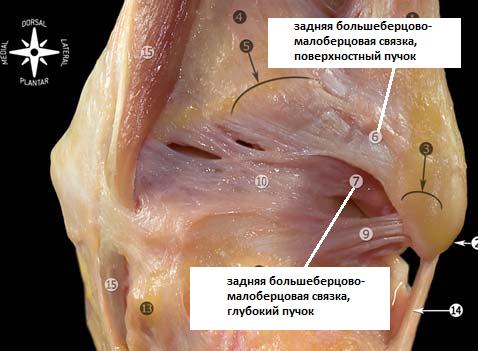
Немного анатомии
Надпяточную кость формирует одна из частей губчатой предплюсны. Ее формирует головка, тело и соединяющая шейка. Головка смыкается с ладьевидной костью, тело, покрытое на 60% суставным хрящом, сочленяется с латеральной и задней лодыжкой наподобие вилки. У тыльного отростка имеются боковые и медиальные бугорки соединяющиеся сухожилием. Суставы снабжаются кровью из малоберцовой, задней, большеберцовой артерии и ее веток. Из-за уникальной анатомической архитектуры после травмы, окклюзии периферических артерий происходит патологическая ишемия. Состояние сопровождается субъективными симптомами некроза таранной кости голеностопного сустава.
Причины и признаки
Патологию провоцируют: красная волчанка, артрит, болезнь Гоше, анемия, сахарный диабет. Также к асептическому некрозу приводят:
эмболия;
тромбоз;
употребление вазоактивных лекарств;
проблемы с липидным метаболизмом;
внутрикостное давление;
нагрузка на большеберцовые кости, резкое сгибание подошв, поражающие магистральные сосуды.;
Симптомы некроза из-за схожести болевых признаков болезнь часто принимают за артроз. Разница состоит в быстрой прогрессии субъективных признаков и возрасте пациентов. Повреждение голеностопных суставов чаще случается у активных людей 20-45 лет. Основные симптомы посттравматического асептического некроза левой таранной кости:
нарастающие болезненные ощущения в лодыжке;
появление отека и хромоты.
При прогрессирующих признаках необходима медицинская помощь, иначе заболевание приведет к инвалидности.
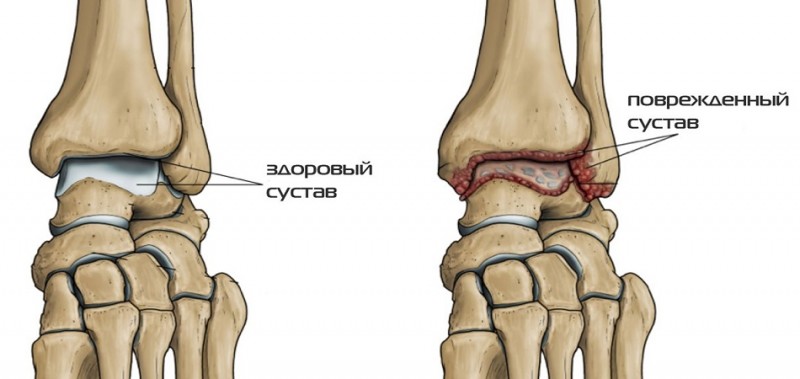
Стадии развития и уровни поражения сустава при некрозе
Степень деструкции при нарушении артериального кровотока связана с функциональностью коллатералей, обеспечивающих кровоснабжение тканей. Заболевание протекает в 3 фазы:
Тотальная характеризуется омертвлением клеток на 90-100%.
Локализационная — онемением наружной поверхности лодыжки.
Глубокая поражает базальные слои ткани.
Классификация по стадиям
Признаки асептического некроза голеностопного сустава помогают определить степень поражения. Более точные сведения дает рентгенограмма, по которой специалист точно определяет фазу заболевания.
I –начальная субарахноидальная компрессия поражает 10% костной ткани. Болезнь не ограничивает движения, периодически дает о себе знать после нагрузок.
II — частичная фрагментация отдельного участка, появление сильных болей, трещин.
III — поражение кости на 40- 50%.
IV — тотальное разрушение и омертвение клеток с расслоением хряща, деструктивные изменения в большеберцовой кости. Фрагментация приводит к потере функциональности ног. Больному с некрозом таранной кости без операции уже не обойтись.
Технология лечения асептического некроза таранной кости в СтопартрозеЕсли у вас имеются похожие проблемы, обращайтесь в клинику. У нас работают травматологи, ортопеды, физиотерапевты с 15-20-летним стажем, специализирующиеся на терапии суставных заболеваний. В день обращения врачи снимают симптоматику, оказывают первую помощь.
Диагностика
Врачи выяснят этимологию болезни, проводят внешний осмотр, назначают информативное обследование. Эти меры необходимы для составления клинической картины и индивидуальной терапевтической программы. Инструментальная диагностика заключается в проведении рентгенографии, МРТ, КТ, биохимии крови. Аномальные изменения в суставах специалисты обнаруживают уже в первую неделю. Для подтверждения диагноза через 5 дней проводят микроскопические тесты, еще раз подтверждающие локальное омертвение тучных клеток.
Методы лечения
Как лечить болезнь Кинбека? Лечение, как правило, зависит от того, насколько своевременно эта болезнь была диагностирована. На начальных этапах проводят консервативную терапию.
Лучезапястный сустав иммобилизируют гипсовой лонгетой в положении небольшого разгибания кисти, выполняют физиотерапевтические процедуры. Противовоспалительные препараты, такие как «Ибупрофен» или «Аспирин» помогут в снятии отека и купировании боли на ранних стадиях.
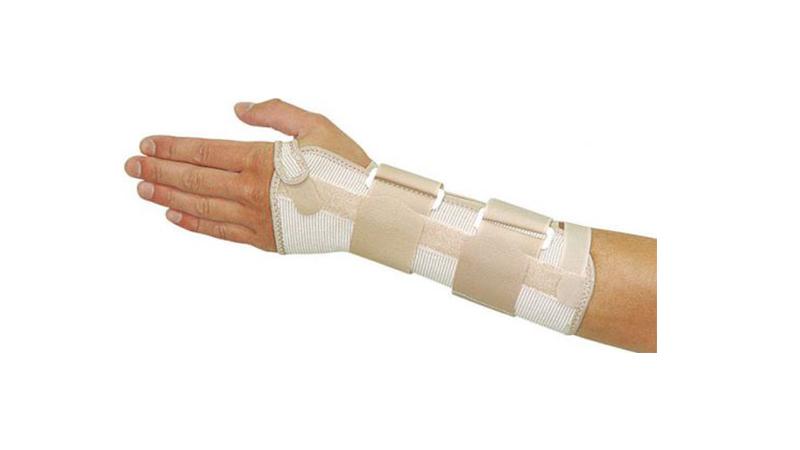
Народные средства
Улучшению кровотока способствует использование согревающих компрессов. Под их воздействием происходит равномерное и длительное расширение сосудов, увеличивается кровоток в кожи и глубоко лежащих тканях, вследствие чего уменьшается воспаление и отек тканей. Это приводит к снятию спазма мышц, ослаблению или исчезновению болей.
Лечение народными средствами включает в себя такие процедуры:
- Можно пользоваться обычной грелкой или мешочком с песком или гречневой крупой.
- Несколько листьев алоэ перемолоть в мясорубке и отжать из них сок. К полученной жидкости добавить по 100 г водки и меда. Все смешать и хранить в темном месте. Полученным раствором смачивать ткань и ставить компрессы (желательно на ночь). Утром теплой водой остатки лечебной смеси необходимо смыть.
- Хорошо применять тертый хрен или редьку. Для смягчающего эффекта хорошо в компресс добавить сметану.
- Взять 0,5 стакана цветов ромашки аптечной и столько же черной бузины, залить небольшим количеством кипятка. Укутать и оставить настаиваться на 15 минут. После этого слить воду и полученный жмых положить в мешочек из ткани. Приложить к больному месту и тепло укутать.
Хирургия
Когда все принятые консервативные меры оказываются неэффективны, а также на поздних стадиях заболевания врачи ставят вопрос об оперативном вмешательстве. Вид операции зависит от стадии заболевания и уровня активности пациента.

Ревалискуляция
Это оперативное вмешательство означает либо восстановление, либо увеличение кровоснабжения к лунообразной кости. С этой целью берут кусочек кости с входящими в нее кровеносными сосудами из нижней части лучевой кости и пересаживают в полулунную кость. Возможна и свободная пересадка кровоснабжаемого костного лоскута из гребня подвздошной и пястной костей.
Эту операцию относят к микрохирургическим: она сложна в техническом плане. После нее кисть иммобилизуют лонгетой или ортезом на 3-4 недели, чтобы пересаженная кость прижилась и кровоток восстановился. Реваскуляризация — эффективный вариант для болезни Кинбека на 1 и 2 стадии.
Остеотомическая коррекция
Остеотомия лучевой кости при болезни Кинбека проводится, если у пациента врожденная короткая локтевая кость, что приводит к повышенному давлению на полулунную кость. В результате укорочения лучевой кости или изменения ее угла наклона нагрузка распределяется равномерно.
Положительные результаты приносят реконструктивные операции с перемещением головки головчатой кости и частичным артродезом запястья. Иммобилизация после оперативных вмешательств продолжается до 12 недель.
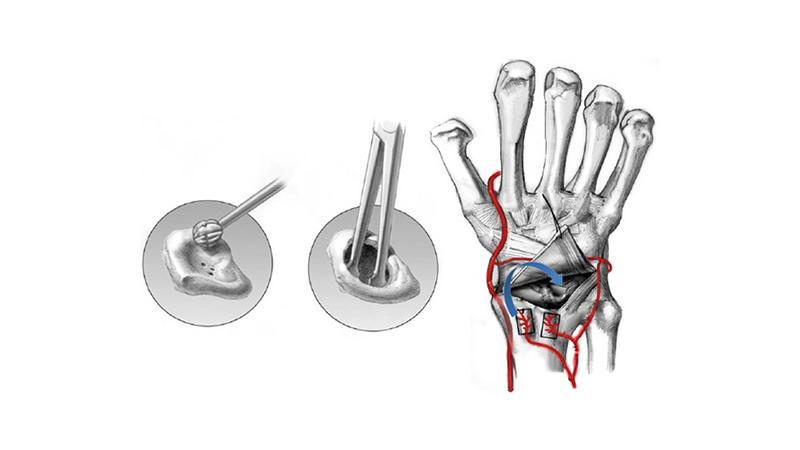
Физиотерапевтические мероприятия показаны как на начальных этапах заболевания, так и после операции. Если больному назначается консервативная терапия с иммобилизацией, то применяют: фонофорез, электрофорез с 10% раствором мумие, грязелечение, парафинотерапию, радоновые ванны, массаж. После операции рекомендованы лечебная гимнастика, массаж, теплые ванны.
Диагностика и лечение патологии
Установление диагноза начинается с осмотра пациента врачом и подробного опроса его. Ортопед проводит пальпацию пораженного участка конечности, проверяет динамические качества сустава. Затем больному рекомендуется пройти инструментальную диагностику, которая поможет подтвердить или опровергнуть предварительное заключение врача. В число диагностических процедур входит:
- Рентгенологическое обследование пораженного участка конечности,
- Ультразвуковое исследование (УЗИ) костной ткани,
- Магнитно-резонансная томография (МРТ) сустава и хрящевой оболочки,
- Компьютерная томография (КТ).
Также проводятся общие анализы крови (ОАК), ее биохимического состава, специализированные тесты, позволяющие выявить гормональный уровень. Исходя из полученных данных, назначается курс терапевтических процедур.
Лечение остеохондропатии костей включает, как консервативные, так и оперативные методики. Хирургическое вмешательство показано в редких случаях, при отделении пораженного участка от основной части кости. Чаще проблема решается при помощи медикаментозных и физиотерапевтических процедур.
Фармацевтическая часть курса при сильных болях в кости включает применение нестероидных противовоспалительных препаратов (НПВП) в форме мази – Диклофенак, Кетопрофен, Инлометацин. Также необходимо употреблять комплекс витаминов и микроэлементов, способствующих активизации регенеративных процессов.
Но основной упор делается на физиотерапию. При поражении головки бедренной кости рекомендуется скелетное вытяжение с грузом. Если пострадали плюсневые (ладьевидные) кости стопы, накладывается специальный гипсовый «сапог», в дальнейшем необходимо ношение обуви с супинатором. Также важная роль в лечебном процессе отводится массажу и лечебной физкультуре при остоеохондропатии плюсневой кости и других участков скелета.
При соблюдении назначений ортопеда высока вероятность выздоровления. Для предотвращения рецидивов болезни костей нужно вести здоровый образ жизни, соблюдать умеренную физическую активность, избегая перегрузок и травм, следить за весом тела, проходить регулярные профилактические осмотры.
https://youtube.com/watch?v=rzJH_T5pnv8
Причины
Аваскулярный некроз —, заболевание дегенеративно-дистрофического характера, сопровождающееся процессом омертвления тканей.
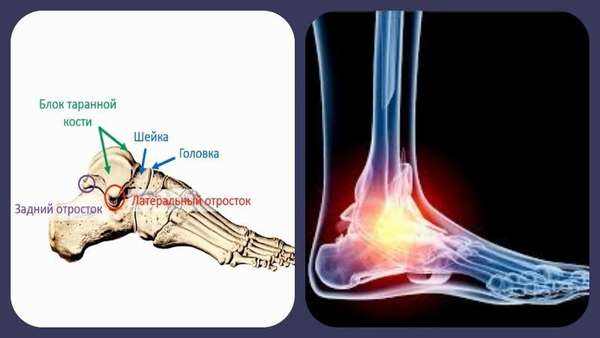
Механизм развития патологии связан с нарушением кровообращения и процесса питания костной ткани.
Поскольку кость —, живая ткань, пронизанная сетью капилляров, то ей необходим постоянный приток крови, питательных веществ, кислорода. Это позволяет ей постоянно обновляться и развиваться.
При нарушении этих естественных процессов, происходит отмирание клеток, а при отсутствии лечения, полное разрушение кости.
Патологический процесс обычно локализуется в участке головки кости в зоне соединения с суставом.
Поражению подвергаются чаще всего крупные кости: бедренная, плечевая. Но нередко наблюдается возникновение асептического некроза таранной кости голеностопного сустава.
Причины развития данного недуга связаны со сбоем питания кости, который может быть спровоцирован различными факторами:
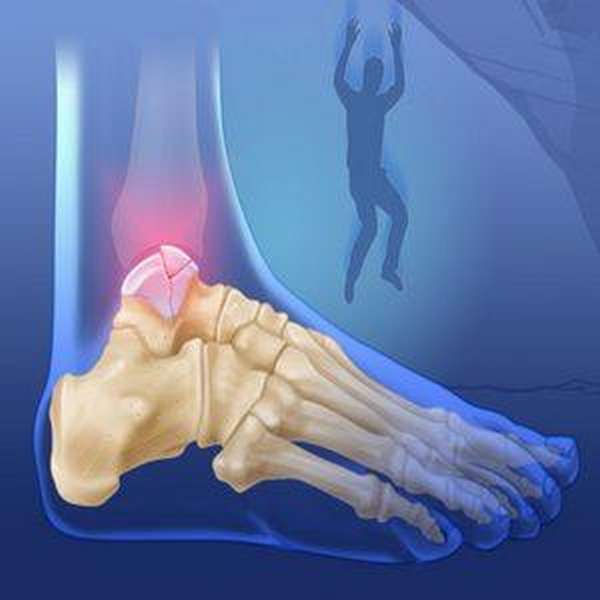
- Травмы —, ушиб, перелом, оперативное вмешательство.
- Длительная терапия сильными гормональными препаратами.
- Нарушение метаболизма, лишний вес.
- Аутоиммунные заболевания.
- Вредные привычки, в особенности злоупотребление спиртными напитками.
- Определенные медицинские манипуляции (химиотерапия, лучевая терапия).
- Повышенные физические нагрузки.
- Патологии позвоночника.
- Перепады показателей атмосферного давления (у дайверов).
Также увеличить риск развития патологии могут такие недуги как сахарный диабет, волчанка, болезнь Гоше, серповидно-клеточная анемия.
Однако в ряде случаев определить точную причину развития остеонекроза не удается. Недуг может возникать без видимых на то причин.
Важные факты о синдроме запястного канала
В феврале 2016 года Американская Ассоциация Ортопедов опубликовала доказательные клинические рекомендации для туннельного синдрома:
- Атрофия тенара позволяет уверенно подтверждает наличие синдрома запястного канала, однако отсутствие этого признака не исключает диагноз.
- Туннельный синдром требует комплексной диагностики. Только сочетание симптомов, характерной истории заболевания и данных ЭНМГ подтверждает диагноз, но никак не каждый из этих методов в отдельности.
- Рутинное использование МРТ не имеет смысла.
- Диагностическое анкетирование в сочетание с электрофизиологическим исследованием может помочь в постановке диагноза.
- Следующие факторы увеличивают риск развития синдрома карпального канала: менопауза, запястный индекс (отношение ширины и толщины), ревматоидный артрит, психосоциальные факторы, тендинопатии дистальных отделов верхней конечности, работа с положением рук над головой, длительная работа на конвейере или за компьютером, воздействие вибрации, постоянные повторяющиеся захваты.
- Физкультура/упражнения снижают риск развития синдрома.
- Применение оральных контрацептивов или гормональная заместительная терапия не оказывают влияния на увеличение или снижение вероятности синдрома карпального канала.
- Использование фиксирующей запястье в нейтральном положении шины достоверно улучшает состояние пациента.
- Блокады со стероидами достоверно оказывают положительный эффект.
- Магнитотерапия не должна применяться для лечения синдрома запястного канала.
- Нет пользы от системного приема медикаментов (диуретиков, габапентина, астаксантина в капсулах, нестероидных противовоспалительных средств или пиридоксина) в сравнении с плацебо.
- Применение стероидов в таблетированной форме может улучшить состояние пациента в сравнении с плацебо.
- Фонофорез с кетопрофеном может вызвать снижение боли в сравнении с плацебо.
- Хирургическое рассечение ладонной связки вызывает исчезновение симптомов и улучшение функцию кисти.
- Оперативное лечение более эффективно на сроке в 6 и 12 месяцев в сравнении с шинированием, противовоспалительной терапией или блокадой со стероидами.
- Рутинная иммобилизация после операции не имеет преимуществ и не рекомендуется.
- Дополнительные хирургические манипуляции, такие как эпиневротомия, невролиз, синовэктомия сухожилий сгибателей, удлинение или реконструкция удерживателя сгибателей (ладонной связки) не дают преимуществ в рутинной практике.
- Специальная реабилитация после операции на запястном канале не дает преимуществ при оценке отдаленных результатов.
ul
Локализация асептического остеонекроза.
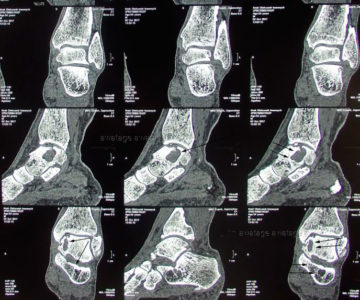
Асептический некроз таранной и пяточной кости. Собственное наблюдение. МЦ “Аватаж”.
Чаще всего асептический некроз кости поражает головку бедренной кости, хотя некрозу могут быть подвержены также
- коленные суставы (мыщелки бедренной кости),
- головка плечевой кости,
- ладьевидная кость запястья
- таранная кость стопы.
Если очаг некроза достигает большой величины, то, например, бедренная кость теряет свою механическую прочность и не может больше выдерживать вес тела человека. В какой-то момент времени поверхность головки бедра становится настолько хрупкой, что сминается по типу яичной скорлупы под обычной нагрузкой (например, при ходьбе). Такое сминание называется коллапсом головки бедра и сопровождается резкой и сильной болью в тазобедренном суставе. Если природа остеонекроза не травматическая, то до 70% больных, пораженных им, имеют двустороннее заболевание.
Асептический некроз бедренной кости диагностируется у мужчин в 4-5 раз чаще, чем у женщин. А асептический некроз мыщелков бедренной кости с поражением коленного сустава встречается и у мужчин и у женщин, но чаще у женщин в пожилом возрасте.
Диагностика асептического некроза полулунной кости
В диагностике асептического некроза полулунной кости исключительно велика роль рентгенологического исследования; по существу, именно оно является решающим для диагностики. Между тем, достаточно достоверные рентгенологические признаки асептического некроза очень часто появляются через многие месяцы после начала первых клинических симптомов заболевания. Неспецифичность жалоб и клинических симптомов и позднее появление достаточных рентгенологических признаков не позволяют установить правильный диагноз достаточно рано и, в соответствии с этим, принять должные меры по лечению и рациональному трудоустройству больного. Выше отмечалось, что заболевание обычно развивается после 3 лет работы в данной профессии. Однако принимать эту цифру за абсолютный критерий нельзя. Имеется не так уже мало случаев, когда болезнь Кинбека начинает развиваться уже спустя несколько месяцев после начала определенной работы и к тому же у совсем молодого человека. Элькин М.А. приводит соответствующее наблюдение:
Б„ 24 лет, в 1964 г., сразу после демобилизации из армии, поступил на судостроительный завод гибщиком красномедных, стальных и алюминиевых труб. Помимо ручной гибки, требующей больших усилий правой руки, ежедневно по 2 часа работает с пневматическим молотком. В прошлом ничем не болел. Через 2 месяца после начала работы на заводе появились ноющие и грызущие боли в правом лучезапястном суставе, которые постепенно усиливались. Был установлен тендовагинит разгибателей правой кисти. Лечился около месяца по больничному листу, временно переводился на облегченную работу. Вскоре после возвращения на постоянную работу боли в руке усилились, появилась припухлость на тыльной поверхности правого запястья. Через 1 год и 4 месяца после работы на заводе (14 месяцев от начала заболевания) прислан к нам на консультацию с диагнозом «болезнь Кинбека (?)». Отчетливая припухлость в проекции полулунной кости, резкая болезненность при пальпации ее, ограниченна и болезненна флексия и экстензия правой кисти.
Деформация и фрагментация правой полулунной кости и начальные явления деформирующего остеоартроза (рентгенограмма).
На рентгенограмме — отчетливое уплощение, деформация и фрагментация правой полулунной кости с нерезким регионарным’ остеопорозом и начальными явлениями деформирующего остеоартроза. Длительное лечение иммобилизацией кисти, новокаиновыми блокадами, парафином оказалось безрезультатным. Больной признан ограниченно трудоспособным, получил профессиональную инвалидность III группы и перешел на работу диспетчера.
Классификация
1. Остеохондропатии эпифизов трубчатых костей — плечевой кости (болезнь Хасса), грудинного конца ключицы, пястных костей и фаланг пальцев кисти (болезнь Тиманна), головки бедренной кости (болезнь Легга-Кальве—Пертеса), головки II—III плюсневых костей (болезнь Келера II).
2. Остеохондропатии коротких губчатых костей — тел позвонков (болезнь Кальве), полулунной кости кисти (болезнь Кинбека), сесамовидной кости I плюснефалангового сустава, ладьевидной кости стопы (болезнь Келера I).
3. Остеохондропатии апофизов (апофизиты) — юношеский апофизит позвонков (болезнь Шейермана—May), апофизит тазовых костей, бугристости болыпеберцовой кости (болезнь Осгуда—Шлаттера), надколенника (болезнь Ларсена—Юхансона), лонной кости, бугра пяточной кости (болезнь Хаглунда—Шинца), апофизит плюсневой кости (болезнь Излена).
4. Частичные клиновидные некрозы суставных концов костей (рассекающий остеохондроз) головки плечевой кости, дистального эпифиза плечевой кости, медиального мыщелка дистального эпифиза бедренной кости (болезнь Кенига), тела таранной кости (болезнь Хаглунда—Севера).
Лечение
Рис. 2. Схема полулунно-лучевого артродеза цилиндрическим трансплантатом при частичном разрушении полулунной кости: 1— образование цилиндрического дефекта (очерченный круг) на стыке между пораженной полулунной и лучевой костями, справа — то же в боковой проекции (пунктиром обозначены границы дефекта); 2—в образованный дефект вставлен цилиндрический трансплантат (заштрихован); кистевой сустав фиксирован спицей, справа— боковая проекция.
Рис. 3. Схема операции замещения удаленной полулунной кости силиконовым эндопротезом (по Свенсону): штифт протеза внедрен в трехгранную кость (протез указан стрелкой).
Рис. 4. Схема реконструктивной операции с перемещением головки головчатой кости и с частичным артродезом кистевого сустава (модификация операции Гранера): 1— пораженная полулунная кость указана стрелкой; уровень остеотомии головчатой кости показан пунктирной линией; 2— удалена полулунная кость, временно извлечена головка головчатой кости; 3—на место полулунной кости реплантирована головка головчатой кости и фиксирована спицей; 4— между фрагментами головчатой кости вставлен цилиндрический костный ауто-трансплантат (заштрихован), кистевой сустав фиксирован спицами.
Лечение длительное время ограничивалось консервативными мероприятиями (иммобилизация, физиотерапия) или удалением полулунной кости. Иммобилизация в циркулярной гипсовой повязке в течение 2— 3 мес. приемлема только на ранних стадиях при «доброкачественном» течении заболевания; в поздних стадиях иммобилизация лишь уменьшает боль и временно приостанавливает разрушение полулунной кости.
Удаление полулунной кости как самостоятельная операция себя не оправдало. Не позднее II—III стадии заболевания рекомендуют операции с укорочением лучевой кости или удлинением локтевой кости; результаты этих вмешательств не всегда надежны и стойки. То же можно сказать об частичной экскохлеации полулунной кости с пломбировкой полости губчатой костью.
Эффективным методом оперативного лечения К. б. являются частичные артродезы (см.) кистевого сустава: полулунно-лучевые, запястные, лучезапястные и др. Применяется выполнение частичных артродезов посредством цилиндрической костной пластики по Ашкенази (рис. 2).
При полных разрушениях полулунной кости, когда сохранить ее не представляется возможным, производят реконструктивно-восстановительные операции. Немало сторонников находит метод замещения полулунной кости силиконовыми эндопротезами (рис. 3); однако Эндопротезирование (см.) не может быть рекомендовано лицам, выполняющим тяжелую ручную работу. Благоприятные результаты приносят реконструктивные операции с перемещением головки головчатой кости и частичным артродезом запястья (рис. 4). Иммобилизация после оперативных вмешательств продолжается от 6 до 12 нед. Восстановительное лечение включает леч. гимнастику, массаж, теплые ванны. Для профилактики деформирующего артроза у части больных показано сан.-кур. лечение спустя 4—6 мес. после операции.
Диагностика асептического некроза полулунной кости
В диагностике асептического некроза полулунной кости исключительно велика роль рентгенологического исследования; по существу, именно оно является решающим для диагностики. Между тем, достаточно достоверные рентгенологические признаки асептического некроза очень часто появляются через многие месяцы после начала первых клинических симптомов заболевания.
Неспецифичность жалоб и клинических симптомов и позднее появление достаточных рентгенологических признаков не позволяют установить правильный диагноз достаточно рано и, в соответствии с этим, принять должные меры по лечению и рациональному трудоустройству больного. Выше отмечалось, что заболевание обычно развивается после 3 лет работы в данной профессии.
Б„ 24 лет, в 1964 г., сразу после демобилизации из армии, поступил на судостроительный завод гибщиком красномедных, стальных и алюминиевых труб. Помимо ручной гибки, требующей больших усилий правой руки, ежедневно по 2 часа работает с пневматическим молотком. В прошлом ничем не болел. Через 2 месяца после начала работы на заводе появились ноющие и грызущие боли в правом лучезапястном суставе, которые постепенно усиливались.
Был установлен тендовагинит разгибателей правой кисти. Лечился около месяца по больничному листу, временно переводился на облегченную работу. Вскоре после возвращения на постоянную работу боли в руке усилились, появилась припухлость на тыльной поверхности правого запястья. Через 1 год и 4 месяца после работы на заводе (14 месяцев от начала заболевания) прислан к нам на консультацию с диагнозом «болезнь Кинбека (?)».
Деформация и фрагментация правой полулунной кости и начальные явления деформирующего остеоартроза (рентгенограмма).
Как правило, в самом начале развития заболевания установить точный диагноз без дополнительного проведения всех необходимых процедур, крайне затруднительно. Чаще всего пациенты жалуются на присутствие болей в запястье, которые усиливаются при физических нагрузках.
На первом этапе диагностика болезни Кинбека предусматривает сбор анамнестических сведений, а затем осмотр. Пальпация определяет болезненность в проекционных областях полулунной кости. При необходимости назначается ряд дополнительных исследований, например, КТ (компьютерную томограмму) в различных проекциях и рентгенологическое обследование.
Симптоматика
Поскольку кость располагается в центральной части стопы, то симптомы нарушения ее целостности схожи с симптоматикой повреждений других костных образований. Характерны следующие симптомы перелома таранной кости стопы:
- сильный отек, охватывающий заднюю поверхность стопы;
- посинение кожи в месте травмы;
- увеличение размера стопы;
- обширная гематома;
- нетипичное изменение формы стопы;
- сильная боль в стопе и во всем голеностопе;
- нарушение подвижности.
Симптомы во многом зависят от локализации перелома:
- при краевом повреждении они неявны и не отличаются сильным болевым синдромом, что часто ошибочно принимается за простой ушиб;
- при травмировании шейки заметна сильная деформация голеностопа;
- при переломе заднего отростка характерна сильная боль в ахилловом сухожилии, обостряющаяся в момент прощупывания.
Кинбека болезнь
Кинбека болезнь (R. Kienbock, австрийский врач-рентгенолог, 1871 —1953) — неспецифическое изолированное поражение полулунной кости кисти, характеризующееся типичной прогрессирующей деформацией дистрофического характера.
Впервые указанная патология полулунной кости обнаружена Пестом (Peste) в 1843 год, расценившим её как следствие перелома. Кинбек в 1910 год первым дал систематизированное клинический, и рентгенологическое описание болезни, назвав её травматической маляцией полулунной кости. В последующем это поражение называли травматическим остеопорозом, кистозной остеодистрофией, хронический оститом, маляцией, асептическим некрозом, остеохондропатией.
Кинбека болезнь чаще встречается у лиц от 20 до 40 лет, занимающихся ручным физических трудом. Женщины заболевают несколько реже мужчин. Правая рука поражается чаще.
Этиология и патогенез Кинбека болезнь не выяснены. Выдвигался ряд гипотез, из которых ни одна не была признана. Считали, что причиной Кинбека болезнь могут быть циркуляторные расстройства вследствие разрыва связок и питающих полулунную кость сосудов; циркуляторные расстройства, возникающие в результате эмболии; однократная травма с первичным компрессионным переломом полулунной кости; хронический травматизация, сопровождаемая микропереломами, и другие. Поскольку Кинбека болезнь обнаруживают у больных с законченным ростом костей и тенденции к последующему восстановлению нормальной структуры полулунной кости не отмечено, поражение не следует, по мнению Д. Т. Рохлина, относить к группе остеохондропатий. Гистологи никогда не находили специфических только для Кинбека болезнь изменений полулунной кости, свидетельствующих об особой костной болезни. Вместе с тем допускалась возможность существования разных причин, приводящих к однотипным деформациям полулунной кости. Современные исследования подтверждают, что Кинбека болезнь не является однородной нозологический формой, а представляет собой полиморфное поражение, в основе которого могут быть асептические некрозы, последствия травматических или патологический переломов.
Заболевание полулунной кости может возникнуть в результате её микротравматизации при хронический перегрузках кистевого сустава (смотри полный свод знаний Лучезапястный сустав), а также вследствие компрессионных переломов при непрямых травмах кистевого сустава и патологический переломов при нераспознанных фиброкистозных дефектах полулунной кости. Предрасполагающим фактором является минус-вариант локтевой кости (высокое стояние её головки), встречающийся при Кинбека болезнь в 8—12 раз чаще, чем в норме. Роль вывихов полулунной кости в возникновении Кинбека болезнь отвергается.
Патологическая анатомия. Основные изменения полулунной кости носят дистрофический характер. Различают пять стадий болезни. I стадия — начало дистрофического процесса в костном веществе при сохранности формы полулунной кости. Во II стадии происходит умеренная деформация её в результате импрессионных переломов со сдавлением костных балок. В III стадии идёт рассасывание костной ткани на границе с участками некроза и замещение их фиброзной тканью; при этом целость хряща и субхондральной пластинки нарушается преимущественно с проксимальной суставной поверхности полулунной кости, прогрессирует деформация. В IV стадии нарастает деформация и происходит вертикальная фрагментация полулунной кости. В V стадии возникают вторичные изменения в виде деформирующего артроза лучезапястного сустава. Последовательный переход одной стадии в другую наблюдается не всегда. В части случаев процесс заканчивается незначительной деформацией полулунной кости («доброкачественная» форма), в других — быстро наступает сплющивание и фрагментация её («злокачественная» форма). Чёткая корреляция между рентгеноморфологическое и клинический, картиной заболевания отсутствует.
Клиническая картина. Первые признаки заболевания — ощущение дискомфорта, непостоянные боли в основании кисти при форсированных движениях и перегрузках. Боли в покое не типичны. Нередко начало Кинбека болезнь протекает скрыто. Острая боль впервые возникает в результате патологический перелома полулунной кости. Постепенно боли при движениях и нагрузках становятся интенсивнее и продолжительнее, хотя возможны и ремиссии.
Диагноз
Рис. 1. Рентгенограммы кистевого сустава (слева в прямой проекции, справа — в боковой) при болезни Кинбека в стадии фрагментации: стрелками указана пораженная полулунная кость.
Клинический диагноз в начальной стадии заболевания затруднителен, однако при соответствующих симптомах (непостоянные боли в основании кисти, локальная болезненность в области полулунной кости, усиление боли при предельном сгибании и разгибании кисти) можно предположить К. б.
Решающим для установления диагноза является рентгенография, но при этом исследовании изменения полулунной кости можно обнаружить не ранее 2—3 мес. от начала заболевания. На рентгенограмме характерно изменение формы и повышение плотности тени полулунной кости. Тень ее приобретает неправильную треугольную форму, высота снижается, контуры кости остаются четкими, но неровными, волнистыми. В стадии фрагментации кость делится на различные по форме, размерам и плотности фрагменты (рис. 1), каждый из которых имеет неровные очертания. В III и IV стадии полулунная кость остается сплющенной, прилежащие отделы суставных щелей расширены. В дальнейшем происходит постепенное неполное восстановление рисунка структуры и формы кости. Полулунная кость остается деформированной, и по краям ее появляются губовидные костные разрастания. Подобные разрастания возникают и на смежных суставных поверхностях (V стадия). Суставная щель из расширенной становится суженной. В отдельных случаях в полости сустава выявляются внутрисуставные тела.
С целью уточнения характера изменений в кости, особенно в начальных стадиях развития патологического процесса, целесообразно применение томографии (см.) и рентгенографии с прямым увеличением изображения.
Дифференциальный диагноз проводят со стенозирующим лигаментитом (см. Тендовагинит), глубоким ганглием (см.), с повреждением полулунно-ладьевидной связки, подвывихом полулунной кости, с фиброкистозным дефектом.
По клинико-рентгенологической картине Кинбека болезнь следует дифференцировать с изолированными поражениями полулунной кости туберкулезного, опухолевого или воспалительного происхождения. При туберкулезном остите и изолированном ревматоидном поражении полулунная кость деформирована и уменьшена в размерах за счет деструкции, а не сплющивания и фрагментации, как это имеет место при К. б. Воспалительный процесс характеризуется остеолитическими изменениями с разрежением рисунка структуры, тогда как при К. б. плотность костной ткани повышена.